در مطلب قبلی در مورد میکروبیوم صحبت کردیم. در این مطلب از دایا اکسیر مرکز فروش مواد شیمیایی در تهران، می خواهیم موضوع باکتریوفاژ را بررسی کنیم. باکتریوفاژ، فاژ یا ویروس باکتریایی نیز نامیده می شود.
فهرست مطالبی که در ادامه به آنها پرداخته شده است:
باکتریوفاژ چیست؟
باکتریوفاژ نوعی ویروس است که باکتری ها را آلوده می کند. در واقع، کلمه “باکتریو فاژ” به معنای”باکتری خوار” است، زیرا باکتریوفاژها سلول های میزبان خود را از بین می برند. همه Bacteriophage ها از یک مولکول اسید نوکلئیک تشکیل شده اند که توسط یک ساختار پروتئینی احاطه شده است. یک باکتریوفاژ خود را به یک باکتری حساس می چسباند و سلول میزبان را آلوده می کند.
پس از عفونت، باکتریوفاژ دستگاه سلولی باکتری را تحت کنترل می گیرد تا از تولید اجزای باکتریایی جلوگیری کند و در عوض سلول را مجبور به تولید اجزای ویروسی می نماید. در نهایت، Bacteriophage های جدید جمع شده و در فرآیندی به نام لیز از باکتری خارج می شوند. باکتریو فاژها گاهی بخشی از DNA باکتریایی سلول های میزبان خود را در طول فرآیند عفونت حذف می کنند و سپس این DNA را به ژنوم سلول های میزبان جدید منتقل می کنند. این فرآیند به عنوان انتقال شناخته می شود.
باکتریوفاژ ویروس باکتریایی نیز نامیده می شوند. باکتریوفاژها به طور مستقل توسط Frederick W. Twort در بریتانیا (۱۹۱۵) و Félix d’Hérelle در فرانسه (۱۹۱۷) کشف شدند. D’Hérelle اصطلاح باکتریوفاژ به معنای “باکتری خوار” را برای توصیف توانایی باکتری کشی آن ابداع کرد. باکتریوفاژها موجودات تک سلولی پروکاریوتی معروف به آرکی را نیز آلوده می کنند.
ویژگی های باکتریوفاژها
هزاران نوع Bacteriophage وجود دارد که هر کدام ممکن است تنها یک نوع یا چند نوع باکتری یا را آلوده کنند. Bacteriophage ها در تعدادی از خانواده های ویروس طبقه بندی می شوند. برخی از نمونه ها عبارتند از:
- Inoviridae
- Microviridae
- Rudiviridae
- Tectiviridae
مانند همه ویروس ها، باکتریوفاژها ارگانیسم های ساده ای هستند که از هسته ای از مواد ژنتیکی (اسید نوکلئیک) تشکیل شده اند که توسط یک کپسید پروتئینی احاطه شده است. اسید نوکلئیک آن ها ممکن است DNA یا RNA باشد و ممکن است دو رشته ای یا تک رشته ای باشد.
معرفی برترین برند مواد آزمایشگاهی، سیگما آلدریچ
ساختار اصلی باکتریوفاژ
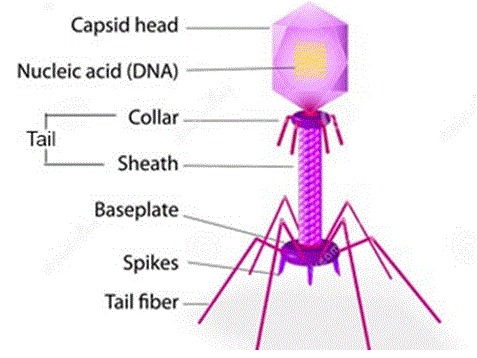
سه شکل ساختاری اصلی برای باکتریوفاژها وجود دارد:
- سر ایکوسادرال (۲۰ وجهی) با دم
- سر ایکوساهدرال بدون دم
- شکل رشته ای.
چرخه زندگی باکتریوفاژها
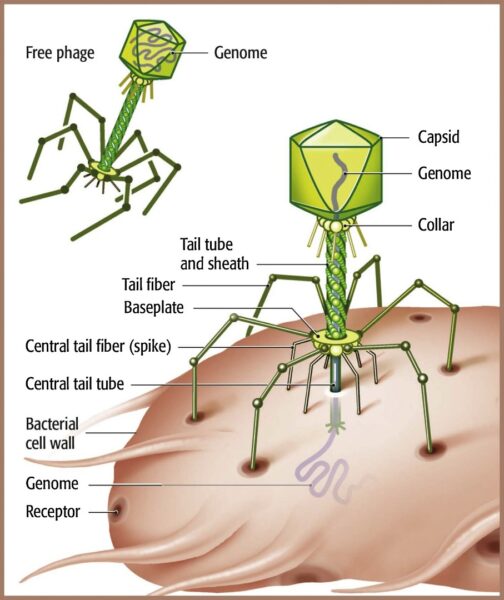
در طول عفونت یک باکتریوفاژ به یک باکتری می چسبد و مواد ژنتیکی آن را وارد سلول می کند. پس از آن، یک باکتریوفاژ معمولاً یکی از دو چرخه زندگی، لیتیک یا لیزوژنیک را دنبال می کند. باکتریو فاژهای لیتیک، سلول را برای ساختن اجزای Bacteriophage در اختیار می گیرند. سپس سلول را از بین برده یا لیز می کنند و ذرات باکتریو فاژ جدید آزاد می نمایند. Bacteriophage های لیزوژنیک اسید نوکلئیک خود را در کروموزوم سلول میزبان وارد کرده و با آن به عنوان یک واحد بدون تخریب سلول، همانند سازی می کنند.
تحت شرایط خاصی می توان Bacteriophage های لیزوژنیک را وادار کرد تا یک چرخه لیتیک را دنبال کنند. چرخه های زندگی دیگر، از جمله شبه لیزوژنی و عفونت مزمن نیز وجود دارد. در شبه لیزوژنی، یک باکتریو فاژ وارد سلول می شود اما نه ماشین تکثیر سلولی را انتخاب می کند و نه به طور پایدار در ژنوم میزبان ادغام می شود. شبهلیزوژنی زمانی اتفاق میافتد که سلول میزبان با شرایط رشد نامطلوب مواجه میشود و به نظر میرسد که نقش مهمی در بقای باکتریوفاژ بازی میکند، تا زمانی که شرایط رشد میزبان دوباره سودمند شود، ژنوم Bacteriophage را قادر میسازد.
نقش در تحقیقات آزمایشگاهی
باکتریوفاژها نقش مهمی در تحقیقات آزمایشگاهی داشته اند. اولین Bacteriophage های مورد مطالعه آنهایی بودند که از نوع(T1) تا نوع (T7) تعیین شده بودند. فاژهای T-even، T2، T4 و T6 به عنوان سیستمهای مدل برای مطالعه تکثیر ویروس استفاده شدند. در سال ۱۹۵۲ آلفرد دی هرشی و مارتا چیس از باکتریو فاژ T2 در آزمایشی معروف استفاده کردند که در آن نشان دادند که فقط اسیدهای نوکلئیک مولکول های باکتریو فاژ برای همانندسازی آنها در باکتری ها مورد نیاز است. نتایج آزمایش این نظریه را تایید کرد که DNA ماده ژنتیکی است. هرشی برای کارش در این زمینه در سال ۱۹۶۹ جایزه نوبل فیزیولوژی یا پزشکی را دریافت کرد.
او این جایزه را با زیستشناسانی به نام سالوادور لوریا و ماکس دلبروک به اشتراک گذاشت که آزمایشهای آنها با باکتریوفاژها T1 در سال ۱۹۴۳ (آزمایش نوسانات) نشان داد که مقاومت فاژی در باکتریها محصول جهش خود به خودی است و پاسخ مستقیمی به عوامل محیطی نیست. Bacteriophage های خاصی مانند لامبدا، مو و M13 در فناوری DNA نوترکیب استفاده می شوند. باکتریوفاژ ϕX174 اولین ارگانیسمی بود که تمام توالی نوکلئوتیدی آن مشخص شد، که توسط فردریک سانگر و همکارانش در سال ۱۹۷۷ انجام شد.
در دهه ۱۹۸۰، بیوشیمیدان آمریکایی، جورج پی اسمیت، فناوری موسوم به نمایش باکتریوفاژ را توسعه داد که امکان تولید پروتئین های مهندسی شده را فراهم کرد. چنین پروتئین هایی با ادغام قطعات DNA خارجی یا مهندسی شده در ژن فاژ III تولید شدند. ژن III پروتئینی را که در سطح ویریون فاژ بیان می شود کد می کند. بنابراین، ژن III پروتئین های همجوشی گرفته شده توسط فاژها بر روی سطوح ذرات ویریون نمایش داده شد. سپس محققان توانستند از آنتیبادیهای توسعهیافته برای شناسایی قطعه پروتئین خارجی برای خالصسازی کشتهای فیوژن فاژ استفاده کنند و در نتیجه توالی ژن خارجی را برای مطالعات بیشتر تقویت کنند.
بیوشیمیدان بریتانیایی گرگوری پی وینتر متعاقباً فناوری نمایش فاژ را برای توسعه پروتئین های آنتی بادی انسانی اصلاح کرد. چنین پروتئین هایی را می توان برای درمان بیماری ها در انسان با خطر کمتری برای ایجاد واکنش های ایمنی خطرناک در مقایسه با آنتی بادی های درمانی قبلی مشتق شده از حیوانات استفاده کرد. Adalimumab (Humira) که برای درمان آرتریت روماتوئید استفاده میشود، اولین آنتیبادی کاملاً انسانی بود که از طریق باکتریوفاژ ساخته شد.
سخن پایانی
در این مطلب به بررسی باکتریوفاژ پرداختیم. Bacteriophage ها نقش مهمی در تحقیقات آزمایشگاهی داشته اند.


4 پاسخ
سپاس جهت مطلب مفیدتان
با سلام
خواهش میکنم. ممنون از ثبت نظرتان.
ممنون عالی
با سلام
ممنون از ثبت بازخورد مثبت شما