در مطلب قبلی در مورد اپی ژنتیک صحبت کردیم. در این مطلب از دایا اکسیر که فروش مواد شیمیایی آزمایشگاهی را انجام میدهد، می خواهیم موضوع آنالیز SDS-PAGE را بررسی کنیم. آنالیز SDS-PAGE یک روش کم هزینه سریع و تکرار پذیر جهت مطالعه پروتئین ها می باشد. این روش به طور معمول برای بررسی مراحل خالص سازی، محاسبه مقدار نسبی و تعیین وزن مولکولی پروتئین ها مورد استفاده قرار می گیرد.
آنالیز SDS-PAGE چیست؟
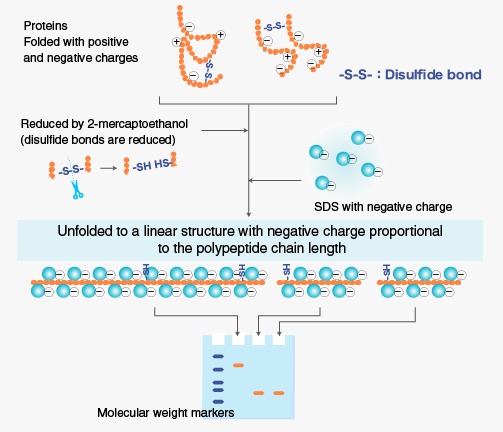
متداول ترین فناوری مورد استفاده برای به دست آوردن جداسازی تحلیلی با وضوح بالا مخلوط پروتئین ها، الکتروفورز ژل پلی آکریل آمید سدیم دودسیل سولفات (SDS-PAGE) است و یکی از دقیقتر و کم هزینه ترین روش های جداسازی و آنالیز پروتئین است.
آنالیز SDS-PAGE (سدیم دودسیل سولفات-پلی آکریل آمید الکتروفورز ژل) یک سیستم الکتروفورتیک ناپیوسته است که توسط Ulrich K. Laemmli ساخته شده است که معمولاً به عنوان روشی برای جداسازی پروتئین هایی با جرم مولکولی بین ۵ تا ۲۵۰ کیلو دالتون استفاده می شود. استفاده ترکیبی از سدیم دودسیل سولفات (SDS) و ژل پلی آکریل آمید اجازه می دهد تا تأثیر ساختار و بار را از بین ببریم و پروتئین ها تنها بر اساس تفاوت در وزن مولکولی آنها جدا می شوند.
آنالیز SDS-PAGE یک روش الکتروفورز است که امکان جداسازی پروتئین بر اساس جرم را فراهم می کند. محیط (ماتریکس) یک ژل ناپیوسته مبتنی بر پلی آکریل آمید است. ژل پلی آکریل آمید معمولاً بین دو صفحه شیشه ای در یک ژل دال قرار می گیرد. اگرچه ژلهای لوله (در استوانههای شیشهای) در طول تاریخ مورد استفاده قرار میگرفتند، اما با اختراع ژلهای slab راحتتر، به سرعت منسوخ شدند. SDS-PAGE در ترکیب با رنگ پروتئین به طور گسترده در بیوشیمی برای جداسازی سریع و دقیق و تجزیه و تحلیل بعدی پروتئین ها استفاده می شود. هزینه ابزار و معرف نسبتاً پایینی دارد و روشی آسان برای استفاده است.
میتوانید محتوای این مطلب را به صورت صوتی گوش دهید
علاوه بر این، آنالیز SDS-PAGE در ترکیب با وسترن بلات برای تعیین وجود یک پروتئین خاص در مخلوطی از پروتئین ها یا برای تجزیه و تحلیل تغییرات پس از ترجمه استفاده می شود. اصلاحات پس از ترجمه پروتئین ها می تواند منجر به تحرک نسبی متفاوت (یعنی تغییر باند) یا تغییر در اتصال آنتی بادی شناسایی مورد استفاده در وسترن بلات شود (یعنی یک نوار ناپدید یا ظاهر شود).
در طیفسنجی جرمی پروتئینها، آنالیز SDS-PAGE یک روش پرکاربرد برای آمادهسازی نمونه قبل از طیفسنجی است که عمدتاً از هضم در ژل استفاده میکند. در مورد تعیین جرم مولکولی یک پروتئین، آنالیز SDS-PAGE کمی دقیق تر از اولتراسانتریفیوژ تحلیلی است، اما دقت کمتری نسبت به طیف سنجی جرمی دارد.
در تشخیص پزشکی، آنالیز SDS-PAGE به عنوان بخشی از آزمایش HIV و برای ارزیابی proteinuria استفاده می شود. در آزمایش HIV، پروتئینهای HIV توسط SDS-PAGE جدا میشوند و در صورت وجود در سرم خون بیمار، توسط وسترن بلات با آنتیبادیهای اختصاصی HIV شناسایی میشوند. آنالیز SDS-PAGE برای proteinuria سطوح پروتئین های مختلف سرم را در ادرار ارزیابی می کند، به عنوان مثال: آلبومین، آلفا-۲-ماکروگلوبولین و IgG.
روش انجام آنالیز SDS-PAGE
آنالیز SDS-PAGE شامل دناتوره کردن اولیه پروتئین های جزء با یک شوینده آنیونی است که به آنها متصل می شود و به همه پروتئین ها یک بار منفی، متناسب با جرم مولکولی آنها می دهد. این مرحله توسط الکتروفورز از طریق یک ماتریس ژل آکریل آمید متخلخل که پروتئین ها را با وضوح عالی بر اساس جرم مولکولی جدا می کند دنبال می شود.
روش انجام آنالیز SDS-PAGE شامل تهیه ژل، آماده سازی نمونه، الکتروفورز، رنگ آمیزی پروتئین یا وسترن بلات و تجزیه و تحلیل الگوی باندینگ تولید شده می باشد.
پروتئین ها در بستری پر از منفذ از جنس آکریل آمید و بیس آکریل آمید که توسط کاتالیزورهایی نظیر آمونیوم پر سولفات و TEMED پلیمریزه می شود به حرکت در می آیند. درصد ژل اکریل آمید وابسته به جرم مولکولی پروتئین می باشد. ناپیوستگی این تکنیک به دلیل وجود دو درصد ژل مختلف برای جداسازی پروتئین در کنار هم است. ژل بالا یا استکینک که کارش فشرده سازی و ژل پایین یا جداکننده که کارش جداسازی پروتئین بر اساس جرم مولکولی است.
پس از اماده سازی ژل، ژل داخل تانک قرار می گیرد و بافر تانک حاوی گلاسیسن و SDS بر روی ژل داخل تانک ریخته می شود.
سپس نمونه ها با بافر نمونه مخلوط و بر روی چاهک های ژل لود می شوند. در کنار نمونه ها یک مارکر پروتئین به عنوان یک خط کش تشخیصی برای اندازه گیری وزن مولکولی پروتئین مورد استفاده قرار می گیرد. تانک به الکترود و سپس به منبع تغذیه وصل می شود. با گذشت زمان و حرکت پروتئین در ژل فشرده ساز، فشرده سازی پروتئین انجام می گیرد که این به جداسازی بهتر پروتئین در ژل جدا کننده کمک می کند. پس از اتمام ژل، برای ظهور و پیدا شدن باندهای پروتئین ، رنگ آمیزی ژل با رنگ کوماسی بلو انجام می گیرد.
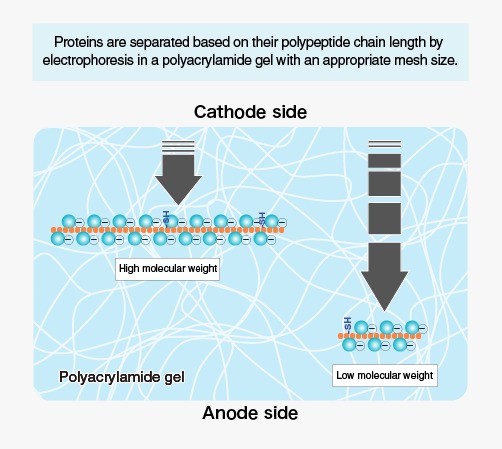
روش به دست آوردن جداسازی پروتئین با وضوح بالا مخلوط های پیچیده توسط آنالیز SDS-PAGE از زمان معرفی آن در چهار دهه پیش اساساً بدون تغییر باقی مانده است. معمولاً برای بررسی حضور، غلظت نسبی و خلوص پروتئینها، جرم مولکولی تقریبی آنها، و در ارتباط با روشهای ایمونوشیمیایی یا طیفسنجی جرمی، هویت آنها و اصلاح کووالانسی احتمالی آنها استفاده میشود. از آنجایی که این روش بر دناتوره سازی پروتئین قبل از الکتروفورز متکی است، نمی توان از آن در تعیین اجزای غیرکووالانسی پروتئین های بومی مانند یون های فلزی یا برای مطالعه ویژگی های عملکرد پروتئین استفاده کرد. مهمتر از همه، مطالعات در سطح پروتئومی با هدف کشف خواص ساختارهای پروتئینی ، از جمله کوفاکتورهای غیرکووالانسی، با SDS-PAGE قابل انجام نیستند.
سخن پایانی
در این مطلب به بررسی آنالیز SDS-PAGE پرداخته شد و آموختیم SDS-PAGE یک سیستم الکتروفورز ناپیوسته است که برای شناسایی و آنالیز پروتئین ها مورد استفاده قرار می گرد. در این روش پروتئین ها با وجود سدیم دو دسیل سولفات دارای بار منفی یکسان می شوند و تنها بر اساس وزن مولکولی از یکدیگر برای آنالیز و تشخیص از هم جدا می شوند.


2 پاسخ
سلام ممنون بابت توضیحاتی که ارائه دادید. اطلاعات بیشتری نیاز دارم چطور دریافت کنم؟
با سلام
ممنون از شما. جهت دریافت اطلاعات بیشتر با کارشناسان شرکت تماس حاصل فرمایید.